ISTH会议速递 | 破局而立,人源化纳米抗体Caplacizumab改善血栓性血小板减少性紫癜患者结局
2022-09-20 17:48:33来源:医脉通阅读:10次
2022年7月9日至13日,第30届国际血栓与止血学会(ISTH)年会在英国伦敦举行。数千名世界领先的血栓、止血和血管生物学专家齐聚一堂,展示和交流该领域的最新研究和突破性成果,从而提升血栓和出血性疾病的诊疗水平。本次ISTH大会公布了血栓性
TTP是一种罕见的、严重的血栓性微血管病,以中重度血小板减少、微血管病性
治疗性血浆置换(PEX)是iTTP的主要治疗方法,PEX引入后,iTTP的死亡率降至10%至20%以下,但在该治疗初始缓解后仍然有25%至50%的患者出现疾病复发或难治3,生活质量下降。Caplacizumab是一种人源化纳米抗体,适用于与标准治疗方式联合治疗成人iTTP患者,为iTTP的管理提供了一种新的方法。
直面困局,TTP仍存在未满足的临床需求
TTP的发病机制主要涉及

图1 TTP的病理生理学
cTTP的发病原因是ADAMTS13基因突变导致血浆ADAMTS13活性缺乏,常在感染、炎症或
国外资料显示,TTP年发病率为2~6/百万,多数TTP患者发病急骤、病情危重,少数患者发病隐匿、临床表现不典型。炎症、感染、妊娠等是诱发TTP常见的原因1。目前治疗方法基于两大支柱:PEX和免疫抑制(IST)。PEX通过清除血液中ADAMTS13抑制物或IgG抗体及其他致病因素、补充缺乏的ADAMTS13而发挥作用;IST可抑制自身抗体形成。尽管该疾病的致死性结局有显著改善,但仍存在一些未满足的需求,这两种治疗的起效相对较慢,不能使血小板计数快速恢复至正常水平,因此在同时使用两种治疗的情况下,iTTP患者的死亡率仍高达20%,另外,iTTP患者中PEX和IST无效的比例高达42%,这类患者的总体预后较差,目前尚未找到可靠的预测危险因素,即使是治疗有效的患者,也有30%~50%会出现复发。另外血浆置换还可能带来血制品治疗常见的过敏、感染等药物不良反应。因此,在iTTP的治疗方面,目前仍存在较大的未满足的临床需求4。
潜精研思,Caplacizumab改善iTTP患者结局
Caplacizumab是治疗iTTP的纳米抗体药物。纳米抗体是在羊驼外周血液中发现的一种天然缺失轻链的抗体。这类抗体只包含1个重链可变区(VHH)和2个常规的CH2及CH3区,与人工改造的单链抗体片段不同,其不易相互粘连、聚集成块,更重要的是,单独克隆并表达的VHH结构具有与原重链抗体相当的结构稳定性以及结合抗原的活性,是已知可结合目标抗原的最小单位,因此被称作纳米抗体4。
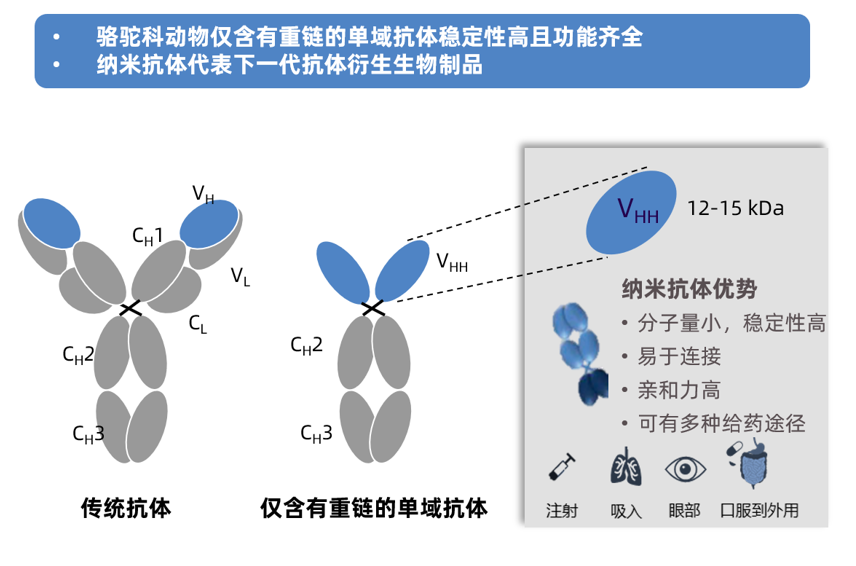
图2 纳米抗体,源自仅含有重链的单域抗体
从机制上看,Caplacizumab大小为28kDa,由两个相同的VWF结合基团组成的二价纳米抗体,通过3-

图3 在iTTP患者中,UL-VWF的蓄积导致血小板通过GP1b受体和VWF上活化的A1结构域结合,从而引起微血管血栓形成(左);Caplacizumab通过与VWF的A1结构域结合,阻断血小板与UL-VWF的相互作用(右)
循证为本,多研究证实Caplacizumab治疗iTTP安全有效
II期TITAN研究:Caplacizumab显著缩短血小板缓解时间、耐受性好5
TITAN是一项II期单盲、随机、安慰剂对照试验,入组了75例iTTP急性发作的成人患者。给药方案为在PEX期间,随机分配为每日皮下注射Caplacizumab 10mg(n=36)或等量安慰剂(n=39),直至PEX结束后30日。试验的主要终点是达到血小板计数缓解的时间,定义为血小板计数初次≥150×109/L。
研究表明,与安慰剂组相比,接受Caplacizumab治疗的患者血小板计数达到缓解时间显著缩短39%,且接受Caplacizumab治疗的患者平均3日后血小板计数恢复到正常范围,而接受安慰剂治疗的患者的血小板计数接近5日恢复到正常范围。Caplacizumab组的出血相关不良事件比安慰剂组更常见(54% vs 38%),但大多数(83%)出血事件为轻度,两组间其他不良事件的发生率相当,未报告Caplacizumab组死亡事件。
III期HERCULES研究:Caplacizumab显著降低iTTP死亡率和并发症发生率6
HERCULES是一项III期双盲、随机、平行、多中心安慰剂对照试验,共入组145例患者。除每日PEX和免疫抑制治疗外,患者随机接受每日Caplacizumab(n=72)或安慰剂(n=73)治疗。在此研究中,患者在首次PEX前接受Caplacizumab或安慰剂时静脉注射,随后在PEX期间接受Caplacizumab或安慰剂时皮下注射,此后持续30日。主要结局是血小板计数达到缓解的时间。
研究表明,与安慰剂组相比,接受Caplacizumab治疗的患者血小板计数达到缓解时间缩短(中位时间:2.69日 vs 2.88日)。在Caplacizumab组患者中未观察到难治性疾病,而在安慰剂组中有3例患者出现难治性。此外,Caplacizumab治疗的患者在一定时间内血小板恢复至正常的可能性是安慰剂的1.55倍。重要的是,Caplacizumab可显著降低iTTP相关死亡、减低重大血栓事件的发生率,且与安慰剂相比,Caplacizumab治疗的患者接受PEX天数相对减少38%,使用的血浆量相对减少41%,重症监护室(ICU)住院时间相对减少65%,住院天数相对减少31%,安全性特征与此前研究一致。
HERCULES事后研究:Caplacizumab可降低iTTP复发率7
HERCULES事后研究是一项多中心、多国、前瞻性研究,旨在评价Caplacizumab在iTTP患者中的长期安全性和疗效,以及在复发患者中重复使用Caplacizumab的安全性和疗效。该研究邀请完成III期HERCULES研究的iTTP患者参加每年两次的访视,持续3年,如果出现iTTP复发,患者可接受开放性的Caplacizumab联合PEX和IST治疗,在整个研究期间共入组了104例意向观察人群,分为仅接受PEX+IST治疗组(n=29)和Caplacizumab+PEX+IST治疗组(n=75)。
研究表明,两组在整个研究期间的不良事件和严重不良事件发生率相似,Caplacizumab+PEX+IST组的患者与仅接受PEX+IST治疗的患者相比,出现TTP相关事件较少(8% vs 38%);Caplacizumab+PEX+IST治疗比仅接受PEX+IST治疗患者的复发率降低(8% vs 28%)。此外,Caplacizumab治疗复发患者的安全性与HERCULES研究中一致,且再次使用Caplacizumab治疗依然有效,未出现新的安全性问题。
小结
本次ISTH大会讨论了TTP治疗中的突出问题和未满足的需求,优化了TTP的治疗,从而改善患者的长期结局。各项研究表明,Caplacizumab是一种与现有标准治疗药物作用机制互补的新药,通过更快地血小板计数正常化,使患者不受病情加重和难治的影响,且耐受性良好,已在临床试验中证实了其疗效和安全性。Caplacizumab为在iTTP的早期关键阶段显著改善预后开辟了希望。
审稿专家简介

韩悦 教授
苏州大学附属第一院血液科副主任、教授、博士生导师
中华医学会血液学分会血栓与止血学组副组长
中华医学会血液学分会委员
江苏省血液免疫学会主任委员
江苏省医学会血液学分会血栓止血学组组长
中国老年医学会血液学分会常务委员
中华医学会血液学分会
中国抗癌协会血液分会委员、细胞治疗与移植学组委员
江苏省“医学重点人才”、“六大高峰人才”、 “333高层次人才”
主持教育部科技进步一等奖、江苏省科技进步一等奖
参考文献
1. 中华医学会血液学分会血栓与止血学组. 血栓性血小板减少性紫癜诊断与治疗中国指南(2022年版) [J] . 中华血液学杂志, 2022, 43(1) : 7-12.
2. 王夕妍, 杨仁池. 血栓性血小板减少性紫癜治疗新进展 [J] . 中华血液学杂志,2019,40 (12): 1055-1059. DOI: 10.3760/cma.j.issn.0253-2727.2019.12.020.
3. Maëlle le Besnerais, Agnès Veyradier, Benhamou Y , et al. Caplacizumab: a change in the paradigm of thrombotic thrombocytopenic purpura treatment[J].
4. 陈霞, 赵建中, 王松. 首个纳米抗体药Caplacizumab的研发历程[J]. 中国临床药理学杂志, 2021, 37(18):5.
5. Peyvandi F, Scully M, Kremer Hovinga JA, Cataland S, Knöbl P, Wu H, Artoni A, Westwood JP, Mansouri Taleghani M, Jilma B, Callewaert F, Ulrichts H, Duby C, Tersago D; TITAN Investigators. Caplacizumab for Acquired Thrombotic Thrombocytopenic Purpura. N Engl J Med. 2016 Feb 11;374(6):511-22.
6. Scully M, Cataland SR, Peyvandi F, Coppo P, Knöbl P, Kremer Hovinga JA, Metjian A, de la Rubia J, Pavenski K, Callewaert F, Biswas D, De Winter H, Zeldin RK; HERCULES Investigators. Caplacizumab Treatment for Acquired Thrombotic Thrombocytopenic Purpura. N Engl J Med. 2019 Jan 24;380(4):335-346.
7. EHA Library. Scully M. Long-term safety and efficacy of Caplacizumab for acquired thrombotic thrombocytopenic purpura (attp): the post-hercules study, 2022, 357158; S294.
该信息仅作医学和科研参考,不建议以任何与您所在国家所批准的处方信息不符的方式使用本产品,本材料仅供医疗卫生专业人士使用。
审批编码:MAT-CN-2216435
“此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场”